2·实验原理和方法
2.1酸析法原理
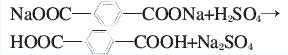
碱减量废水中的对苯二甲酸钠与硫酸作用形成对苯二甲酸。当废液pH值<3时,对苯二甲酸几乎不溶于水,因此会从碱减量废水中析出。
2.2碱减量废水水质分析
2.2.1 COD的测定
在强酸性溶液中,一定量的重铬酸钾氧化水样中还原性物质,过量的重铬酸钾以试亚铁灵作指示剂、用硫酸亚铁铵溶液回滴。根据用量计算水样中还原性物质的量。
2.2.2稀释倍数法色度测定
将样品用光学纯水稀释至用目视比较与光学纯水相比刚好看不见颜色时的稀释倍数作为表达颜色的强度,单位为倍。
2.2.3浊度测定
在25℃下,硫酸肼与六次甲基四胺聚合,形成白色高分子聚合物。以不同浓度的聚合物溶液作为浊度标准液,水样浊度与其相比较而得。
2.2.4对苯二甲酸含量测定
对苯二甲酸溶于氢氧化钠溶液,读取分光光度计A254、A256值,求得(A254-A256)/2。前式的值与对苯二甲酸浓度在一定范围内成直线关系,所以可按其测得的吸光度求出对苯二甲酸的含量。事实上,废水中不含对苯二甲酸,而是以对苯二甲酸钠形式存在。这里所谓的对苯二甲酸含量是指由对苯二甲酸钠换算得到的相应值。
2.3对苯二甲酸特性分析
2.3.1酸值测定
取1g样品,加入吡啶10mL,加热溶解后冷却至室温,加入15mL H2O。以酚酞为指示剂,用0.5mol/LKOH标准溶液滴定。
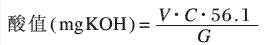
式中,V-KOH标准溶液用量,mL;C-KOH标准溶液浓度,mol/L;G-样品重量,g。
2.3.2灰分测定
取2g样品放入已恒重的20mL坩锅中,在电炉上小心进行碳化。再于马福炉中在800℃下灼烧至恒重。
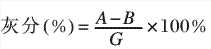
式中,A-样品灼烧的重量,g;B-坩锅重量,g;G-样品重量,g。
2.4絮凝和脱色使用3种不同的有机高分子絮凝脱色剂(1#,2#,3#)。将稀释20倍脱色剂加入1L废水中,搅拌均匀后,静置20min再进行过滤。
2.5酸析
取絮凝脱色后的碱减量废水1L,分别缓慢加入浓硫酸并且不断搅拌,直至pH为2。静止片刻后,废水进行过滤。滤液进行水质分析,而滤饼烘干并测定对苯二甲酸特性。
<<上一页[1][2][3][4]下一页>>
 相关信息
相关信息 






 推荐企业
推荐企业 推荐企业
推荐企业
 推荐企业
推荐企业